Schlüsselwörter: Isotherme Kalorimetrie, TAM, Wärmestrom, Wärmefluss, Lithium-Ionen-Akkumulatoren, Elektrolytzusätze, parasitäre Wärme
MC162-DE
Abstract
Die isotherme Mikrokalorimetrie bietet eine einfache Methode, um die Auswirkungen zu bestimmen, die ein Elektrolytzusatzstoff oder eine Kombination mehrerer Additive auf die parasitären Reaktionen in einem Lithium-Ionen-Akkumulator in seinen unterschiedlichen Ladezuständen hat. In dieser Studie wurde ein hochauflösendes TAM-System mit 12 Mikrokalorimetern verwendet, um Messungen und quantitative Vergleiche des Wärmestroms von Lithium-Ionen-Akkumulatoren durchzuführen, die sich nur in der Konzentration des Elektrolytzusatzes unterschieden. Da in diesem Fall alle anderen Wärmequellen identisch waren, konnte der gemessene Wärmestrom direkt auf die Differenzen bei der parasitären Wärme zurückgeführt werden, die der Zusatzstoff bewirkte. Die Definition der Funktion in Abhängigkeit vom Ladestatus bietet eine einfache und schnelle Methode zur Bestimmung, wo genau und in welchem Ausmaß der Elektrolytzusatz die parasitären Reaktionen reduziert. Ein anschauliches Beispiel lieferte das Experiment zur Bestimmung der Auswirkungen verschiedener Konzentrationen von Vinylencarbonat auf LiCoO2/Graphit-Zellen. Dabei zeigte sich, dass Vinylencarbonat parasitäre Reaktionen über 3,9 V reduzierte und diese Reaktionen mit steigendem Ladezustand weiter verringerte. Die hierin vorgestellte Methode und die Daten wurden veröffentlicht (Quelle 1) und werden mit Genehmigung reproduziert. ©2013, The Electrochemical Society.
EINFÜHRUNG
Lithium-Ionen-Akkumulatoren werden heutzutage für eine zunehmende Anzahl von Anwendungen eingesetzt, die immer höhere Energiedichten und längere Nutzungszeiten erfordern. Eine gängige Methode, um die Haltbarkeit und die Zyklenzahl von Akkus zu erhöhen, sind Elektrolytzusätze. Diese Additive reduzieren die parasitären Reaktionen, die zwischen dem Elektrolyten und dem Elektrodenmaterial auftreten. Die genaue Funktionsweise dieser Zusätze, und an welchem Punkt im Lade-/Entladezyklus sie den größten Nutzen bieten, ist jedoch noch nicht vollständig erforscht. Es besteht daher ausgeprägtes Interesse daran zu bestimmen, welchen spannungsabhängigen Nutzen ein bestimmter Zusatzstoff oder eine Kombination aus mehreren Additiven hat, um herauszufinden, wie sich die Lebensdauer von Lithium-Ionen-Akkumulatoren mit solchen Zusätzen verlängern lässt.
In neueren Studien wurde die Technik der isothermen Mikrokalorimetrie mit elektrochemischen Messungen kombiniert, um das Temperaturverhalten verschiedener chemischer Zusammensetzungen von Lithium-Ionen-Akkumulatoren zu untersuchen.2-9 Kürzlich zeigten Krause et al.10, wie mit dieser Methode die einzelnen wärmeenergetischen Beiträge unterschieden werden können, um die parasitäre Energie zu isolieren. Sie nutzten diese Technik, um den Wärmefluss zwischen Zellen, die sich lediglich durch die Konzentration des Zusatzes unterschieden, qualitativ und quantitativ zu vergleichen. Da in diesem Fall alle anderen Wärmequellen identisch waren, konnten die gemessenen Unterschiede beim Wärmestrom direkt auf die Differenzen bei der parasitären Wärme zurückgeführt werden. Die Definition der Funktion in Abhängigkeit vom Ladestatus bietet eine einfache und schnelle Methode zur Bestimmung, wo genau und in welchem Ausmaß der Zusatz die parasitären Reaktionen zwischen dem Elektrolyten und dem Elektrodenmaterial reduziert. Ein anschauliches Beispiel lieferte das Experiment zur Bestimmung der Auswirkungen verschiedener Konzentrationen von Vinylencarbonat auf eine LiCoO2/Graphit-Zelle. Der Elektrolytzusatz Vinylencarbonat wird weit verbreitet eingesetzt, da er nachweislich die Lebensdauer von Zellen verlängert.11
VERSUCHSAUFBAU
Maschinell hergestellte LiCoO2/Graphit-Pouch-Zellen, 225 mAh (erworben bei Pred Materials Co.), wurden trocken bereitgestellt. Die Beutel wurden mit 0,75 g Elektrolyten gefüllt, bestehend aus 1 M LiPF6 in einer Mischung von 3:7 von Ethylencarbonat und Ethylmethylcarbonat (Novolyte Technologies, heute BASF) sowie variierenden Mengen (0 %, 0,5 %, 2 % und 4 % Gewichtanteil) von Vinylencarbonat-Zusatz (Novolyte Technologies, heute BASF). Die Beutel wurden vakuumdicht verschlossen. Die Elektroden wurden in einer Zentrifuge bei 50 g für 20 Minuten benetzt. Die Zellen wurden anschließend geformt und bei 1,5 V über 24 Stunden bei 40 °C stehengelassen. Dann wurden sie 10 Stunden lang bei 2 mA aufgeladen und anschließend bei 15 mA auf 4,2 V geladen. Danach wurden sie bei 15 mA auf 3,775 V entladen. Anschließend wurden die Zellen aufgeschnitten, um entstandene Gase abzulassen, und erneut versiegelt. Das Laden und Entladen der Zellen im Mikrokalorimeter erfolgte unter Verwendung eines automatisierten Prüfsystems der Serie Maccor 4000 (Maccor Inc.).
Zur mikrokalorimetrischen Messung der isothermen Wärmeströme wurde ein TAM-Kalorimeter (TA Instruments-Waters LLC) bei einer Temperatur von 40,0 °C genutzt. Die Messunsicherheit betrug < ±1,0 μW. Details bezüglich Kalibrierung und Betrieb des Instruments, Hintergrundinformationen und die Methoden werden in Quelle 10 ausführlich besprochen. Das Instrument weist ein Grundrauschen von ungefähr 10 μW auf, und der Basisliniendrift betrug weniger als 500 μW über den Durchführungszeitraum der hier beschriebenen Experimente. [/vc_column_text][/vc_column][/vc_row][vc_row][vc_column][vc_column_text]
ERGEBNISSE UND DISKUSSION
Wärmestrom während der Zyklisierung
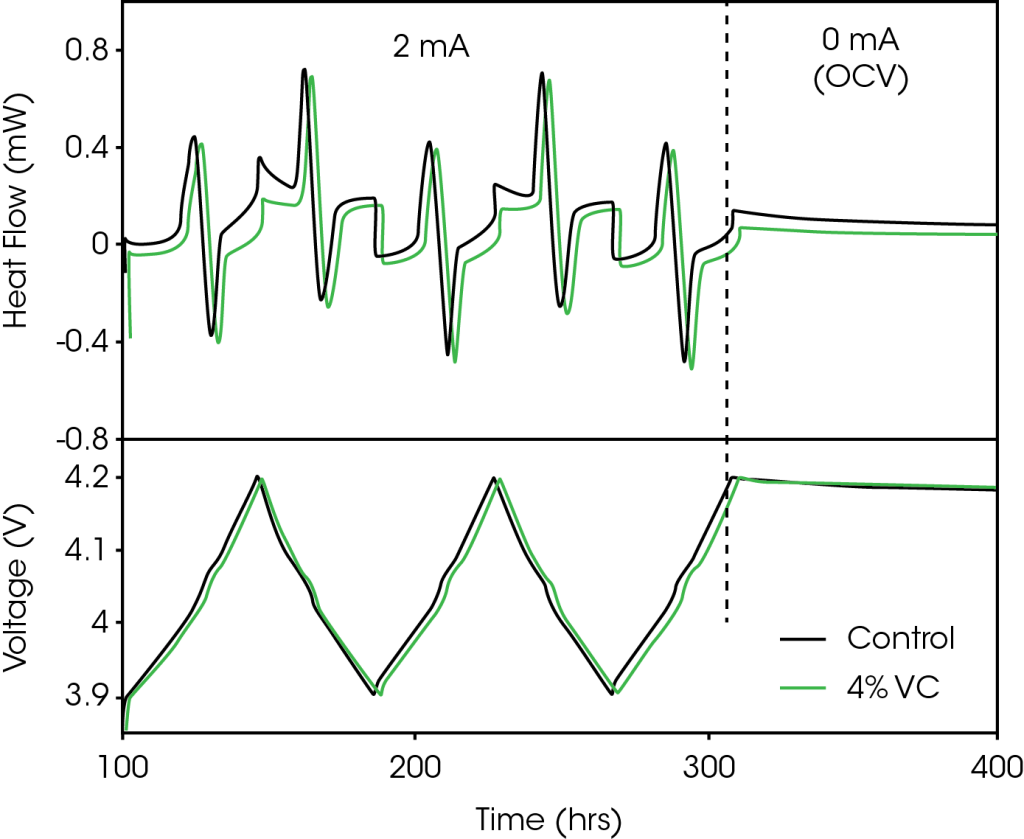
Abbildung 1 zeigt ein repräsentatives Segment des Zyklisierungsprotokolls, das zum Testen der Zellen im Mikrokalorimeter verwendet wurde. Abbildung 1a zeigt den gemessenen Wärmestrom und Abbildung 1b das zugehörige Spannungsprofil. Der Einfachheit halber sind nur die Daten für die Kontrollzelle (ohne Vinylencarbonat) und die Zelle mit 4 % Vinylencarbonat dargestellt. Das Zyklisierungsprotokoll besteht aus den folgenden zwei unterschiedlichen Segmenten, die in Abbildung 1 durch eine senkrechte gestrichelte Linie getrennt sind:
- 2 mA (Laden auf 4,2 V, Entladen auf 3,9 V) x2, Laden auf 4,2 V
- 100 Stunden bei offenem Stromkreis, beginnend bei 4,2 V
Der Wärmestrom der Zelle, der während der Zyklisierung gemessen wird, setzt sich aus Beiträgen dreier Wärmequellen zusammen: Entropie, Polarisierung sowie parasitäre Wärme von der positiven und negativen Elektrode.12 Die Wärmebeiträge aufgrund von Entropie und Polarisierung sind Ausdrücke, die von der Stromstärke abhängen. Von der parasitären Wärme wird angenommen, dass sie nicht mit der Stromstärke in Zusammenhang steht. Sowohl beim Graphit als auch beim LiCoO2 treten während des Ladens und Entladens große Entropieänderungen auf (Transition zwischen Interkalationsstufen beim Graphit13 und Transition zwischen Ordnung und Unordnung beim LiCoO214), die für den Großteil der reversiblen Struktur im Wärmestromprofil in Abbildung 1a verantwortlich sind. Diese Eigenschaften werden in Quelle 7 und 9 ausführlicher beschrieben. Die Polarisierung resultiert sowohl während des Ladens als auch Entladens in einem überwiegend konstanten exothermen Wärmefluss. Der Rest des Signals ist das Resultat parasitärer Wärmeströme.
Die in diesem Experiment verwendeten maschinell gefertigten Pouch-Zellen sind nominell identisch, da sie sich lediglich durch die Menge des hinzugefügten Vinylencarbonats unterscheiden. Die Kapazitätsunterschiede zwischen den Zellen waren in diesem Fall geringer als 1 %. Wenn die Stromstärke schwach genug ist, tragen Entropie und Polarisierung bei allen Zellen zu einer genau gleichhohen Wärmeentwicklung bei. Daher kann davon ausgegangen werden, dass die Unterschiede beim Wärmestrom auf parasitäre Wärme zurückzuführen sind. Abbildung 1a zeigt, dass der Wärmestrom der Zelle mit 4 % Vinylencarbonat geringer ist als der von der Kontrollzelle. Im Interesse der Klarheit ist hier nur ein Ausschnitt dargestellt, aber alle Zellen, die Vinylencarbonat enthielten, wiesen Wärmeströme auf, die niedriger waren als die der Kontrollzellen. Anhand der Funktion der Differenz der Wärmestromänderungen in Abhängigkeit vom Ladezustand werden die Vorteile der isothermen Mikrokalorimetrie deutlich. Sie bietet eine einfache Methode, um die Spannungsabhängigkeit der parasitären Reaktionen und den Nutzen von Vinylencarbonat oder anderen Additiven zu bestimmen. In diesem Beispiel war die parasitäre Wärme des Prüflings mit 4 % Vinylencarbonat merklich geringer als die der Kontrolle.
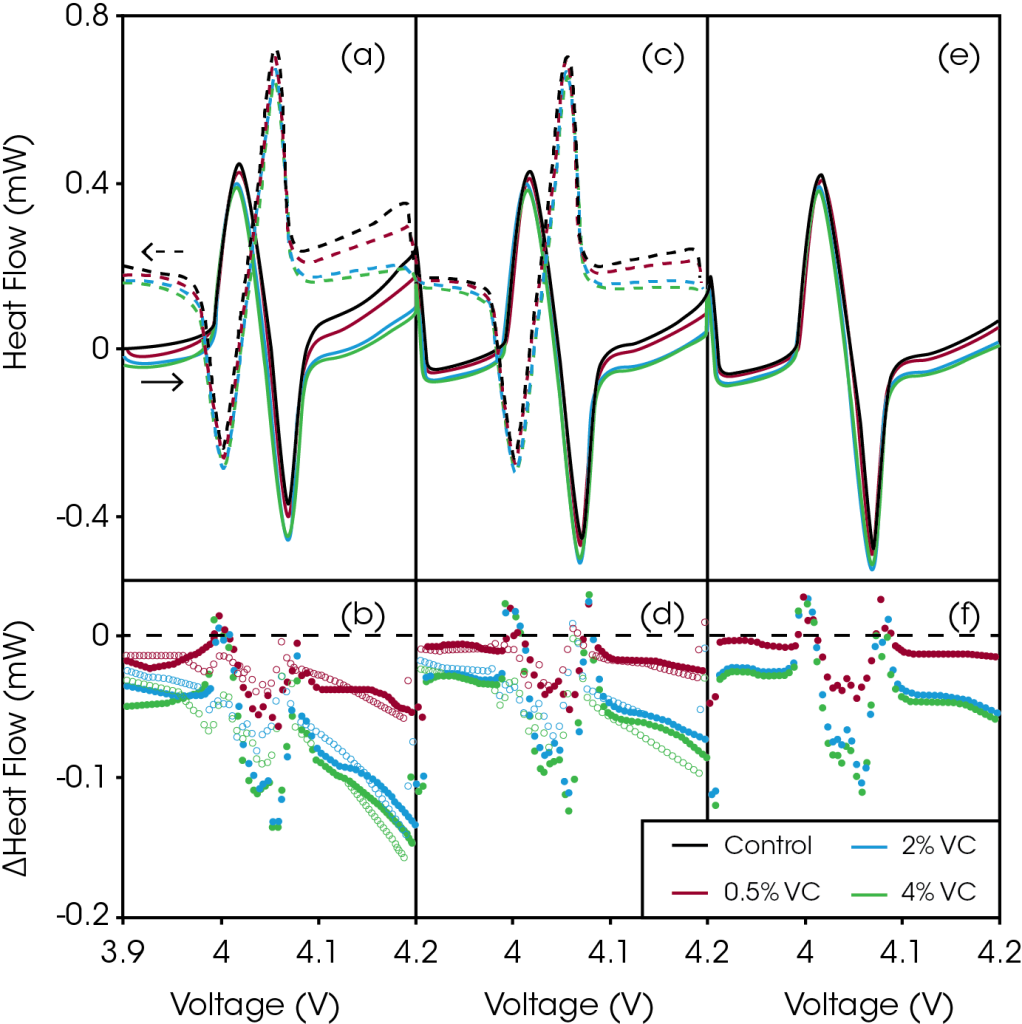
Es ist zu beachten, dass der Wärmefluss aus den Pouch-Zellen selbst bei solchen schwachen Stromstärken zwei bis drei Größenordnungen über dem Grundrauschen des TAM-Mikrokalorimeters lag, sodass die Zellen äußerst genau unterschieden werden konnten. Abbildung 2 zeigt die Funktion des Wärmestroms in Abhängigkeit von der Spannung während Teil 1 des in Abbildung 1 dargestellten Zyklisierungsprotokolls (3,9 V–4,2 V bei 2 mA). Abbildung 2a zeigt den Wärmestrom während des ersten 2-mA-Lade- und Entladevorgangs für Zellen mit zunehmend höheren Mengen von Vinylencarbonat. Es ist deutlich zu sehen, dass mit zunehmender Spannung der Zusatz von Vinylencarbonat den Wärmestrom reduzierte. Insbesondere bei Spannungen über 4,1 V ist eine dramatische Verringerung zu beobachten.
Abbildung 2. Die Bildbereiche (a), (c) und (e) zeigen die Funktion des Wärmestroms in Abhängigkeit von der Spannung während des Ladens (durchgezogene Linie) und Entladens (gestrichelte Linie) bei niedrigen Raten über einen engen Spannungsbereich (3,9 V–4,2 V) im ersten (a), zweiten (c) und dritten (e) Zyklus für die Kontrolle (schwarz), die Zelle mit 0,5 % Vinylencarbonat (rot), die Zelle mit 2 % Vinylencarbonat (blau) und die Zelle mit 4 % Vinylencarbonat (grün). Die Bildbereiche (b), (d) und (f) zeigen die entsprechenden Unterschiede beim Wärmefluss in Abhängigkeit von der Spannung zwischen den Zellen mit Vinylencarbonat und den Kontrollzellen während des Ladens (durchgezogene Linie) und Entladens (gestrichelte Linie) im ersten (b), zweiten (d) und dritten (f) Zyklus. Reproduziert mit Genehmigung von ECS Electrochem Lett., 2, A106-A109 (2013). ©2013, The Electrochemical Society.
Abbildung 2 zeigt die Differenz nach Subtraktion des Wärmestroms der Kontrollzelle (ohne Vinylencarbonat) vom Wärmestrom der Vinylencarbonat-Zellen in Abhängigkeit von der Spannung. Diese Differenz eignet sich gut zur Beurteilung, in welchem Maße der Zusatz die parasitäre Wärme reduziert. Der Wärmestrom der Zellen, die Vinylencarbonat enthalten, wird über den gesamten Spannungsbereich reduziert. Jedoch im ungefähren Wertebereich von 3,98 V bis 4,1 V ist diese Differenz aufgrund leichter Abweichungen im Verlauf der Wärmeprofilkurven nicht zu erkennen, da sich dasLiCoO2 auf der Stufe der Transition zwischen Ordnung und Unordnung befindet. Die Reduzierung des Wärmestroms wird mit zunehmender Spannung immer deutlicher, was darauf hindeutet, dass der Zusatz von Vinylencarbonat parasitäre Reaktionen verringert, die an der positiven Elektrode auftreten. Selbst 0,5 % Vinylencarbonat resultierte bereits in einer signifikanten Verringerung des Wärmestroms um 54 μW bei 4,2 V, während 2 % und 4 % Vinylencarbonat den Wärmestrom bei 4,2 V um 132 μW bzw. 148 μW reduzierten. Die Reduzierung der parasitären Wärme in Abhängigkeit von der Additivkonzentration ist keine lineare Funktion. Die Unterschiede beim Wärmestrom der Zellen mit 2 % und 4 % Vinylencarbonat sind sehr ähnlich, woraus geschlossen werden kann, dass sich bei dieser Zellchemie durch Hinzufügen von mehr als 2 % Vinylencarbonat nur wenig zusätzlicher Nutzen erreichen lässt.
Die Funktionen in den Abbildungen 2c und 2d zeigen den Wärmestrom in Abhängigkeit von der Spannung sowie den entsprechenden Graphen mit den Unterschieden zwischen 3,9 V und 4,2 V für den zweiten Lade- und Entladevorgang. Der Wärmestrom aller vier Zellen reduzierte sich bei allen Spannungswerten leicht, und die Unterschiede bei den Wärmeströmen verringerten sich ebenfalls. In den Abbildungen 2e und 2f sind die gleichen Graphen für den dritten und letzten Ladevorgang dargestellt. Auch hier verringerten sich sowohl die Wärmeströme als auch die Unterschiede beim Wärmestrom. Wie erwartet nahmen die parasitären Reaktionen mit zunehmender Zyklenzahl ab. Nach dem dritten Laden wurde bei 4,2 V der parasitäre Wärmestrom der Zelle mit 0,5 % Zusatz vonVinylencarbonat im Vergleich zur Kontrollzelle um 15 μW reduziert. Der Unterschied der Zelle mit 2 % Vinylencarbonat zur Kontrolle betrug 54 μW, und der Unterschied der Zelle mit 4 % Vinylencarbonat 60 μW.
Wärmestrom bei offenem Stromkreis
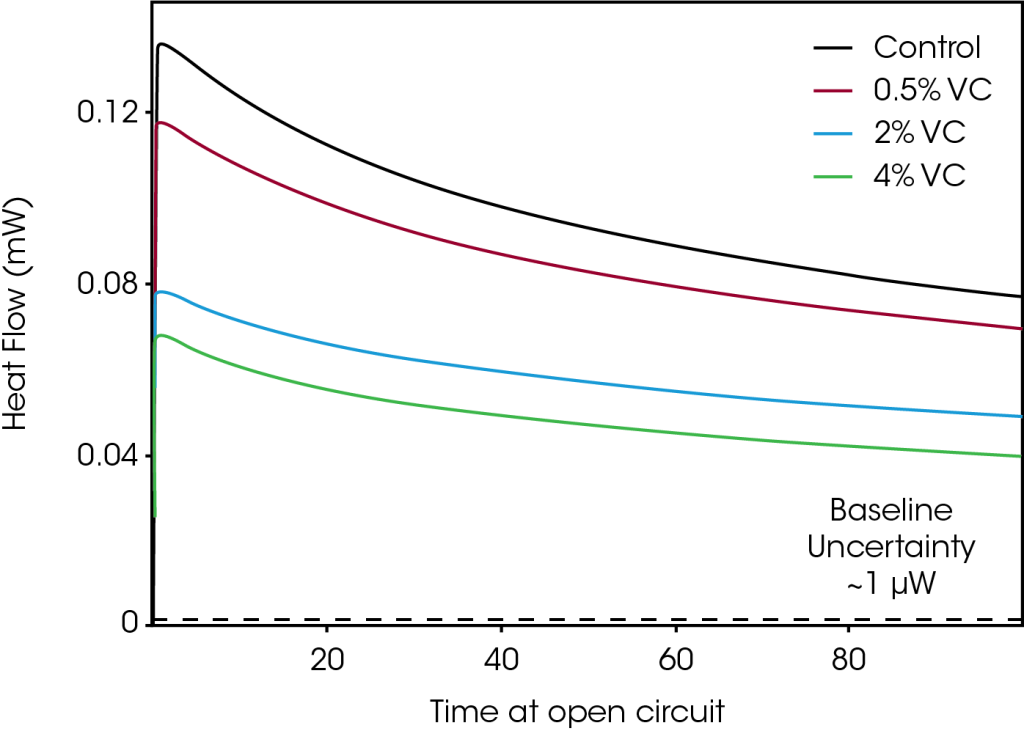
Abbildung 3 zeigt die Evolution des Wärmestroms für die gleiche Gruppe von Zellen, die nach dem Aufladen auf 4,2 V bei Leerlaufspannung belassen wurden (Schritt 2 in Abbildung 1). Da kein Strom an den Zellen anlag, lieferten die Wärmeflussmessungen beim offenen Stromkreis ein direktes Maß des Wärmestroms, der auf parasitäre Reaktionen zurückzuführen war. Mit zunehmender Menge Vinylencarbonat konnte eine deutliche Abnahme der parasitären Wärme beobachtet werden. Dies stimmt qualitativ mit den Ergebnissen in Abbildung 2 überein. Im offenen Stromkreis nehmen die Wärmestromunterschiede der Zellen im Zeitverlauf ab. So beträgt zum Beispiel der Unterschied beim Wärmestrom der Kontrolle und der Zelle mit 4 % Vinylencarbonat nach 5 Stunden Leerlaufspannung 66 μW, doch nach 100 Stunden verkleinert sich diese Differenz auf 31 μW. Dies entspricht der Reduzierung der parasitären Wärme mit der Zyklenzahl (und dementsprechend mit der Zeit), wie in Abbildung 2 gezeigt.
FAZIT
Die isotherme Mikrokalorimetrie ist eine leistungsstarke Technik zur Messung des Spannungsbereichs, in dem ein Zusatz oder eine Kombination mehrerer Additive am wirksamsten ist. Die so gewonnenen Daten tragen zum besseren Verständnis der Elektrolytzusätze bei, sodass die geeignete Additivkombination für eine spezifische Zellchemie und bestimmte Betriebsbedingungen bestimmt werden kann. Der vorliegende Artikel präsentiert ein Verfahren, bei dem die Auswirkungen unterschiedlicher Konzentrationen vonVinylencarbonat auf LiCoO2/Graphit-Zellen untersucht wurden. Der Zusatz von Vinylencarbonat führte zu einer dramatischen Verminderung parasitärer Reaktionen bei hohen Potenzialen, was darauf hinweist, dass Vinylencarbonat parasitäre Reaktionen reduziert, die an der positiven Elektrode auftreten.
LITERATURHINWEISE
- L. E. Downie, K. J. Nelson, R. Petibon, V. L. Chevrier, and J. R. Dahn, ECS Electrochem. Lett., 2, A106–A109 (2013).
- W. Lu, I. Belharouak, D. Vissers, and K. Amine, J. Electrochem. Soc., 153, A2147–A2151 (2006).
- W. Lu, I. Belharouak, J. Liu, and K. Amine, J. Power Sources, 174, 673–677 (2007).
- W. Lu, I. Belharouak, J. Liu, and K. Amine, J. Electrochem. Soc., 154, A114–A118 (2007).
- W. Lu, I. Belharouak, S. H. Park, Y. K. Sun, and K. Amine, Electrochimica Acta, 52, 5837–5842 (2007).
- W. Lu and J. Prakash, J. Electrochem. Soc., 150, A262–A266 (2003).
- Y. Kobayashi, H. Miyashiro, K. Kumani, K. Takei, T. Iwahori, and I. Uchida, J. Electrochem. Soc., 149, A978–A982 (2002).
- J.-S. Kim, J. Prakash, and J. R. Selman, Electrochem. Solid-State Lett., 4, A141–A144 (2001).
- Y. Saito, K. Takano, K. Kanari, A. Negishi, K. Nozaki, and K. Kato, J. Power Sources, 97–98, 688–692 (2001).
- L. J. Krause, L. D. Jensen, and J. R. Dahn, J. Electrochem. Soc., 159, A937–A943 (2012).
- J. C. Burns, N. N. Sinha, D. J. Coyle, G. Jain, C. M. VanElzen, W. M. Lamanna, A. Xiao, E. Scott, J. P. Gardner, and J. R. Dahn, J. Electrochem. Soc., 159, A85–A90 (2012).
- J. R. Dahn, W.R. MacKinnon, J.J. Murray, R.R. Haering, R.S. McMillan, and A.H. Rivers-Bowerman, Phys. Rev. B, 32, 3316–3318 (1985).
- J. R. Dahn, Phys. Rev. B, 44, 9170–9177 (1991).
- J. N. Reimers and J. R. Dahn, J. Electrochem. Soc., 139, 2091–2097 (1992).
DANKSAGUNG
Dieser Artikel basiert auf Beiträgen von L.E. Downie sowie der Mitautoren K.J. Nelson und J.R. Dahn vom Department of Physics and Atmospheric Science, Dalhousie University, Halifax, N.S., B3H 4R2, Kanada im Rahmen des Student Applications Award Program von TA Instruments. Die Verfasser bedanken sich für die Unterstützung dieser Arbeit unter der Schirmherrschaft des Industrial Research Chair in Materials for Advanced Batteries von NSERC/3M Canada. LED und KJN bedanken sich für die finanzielle Unterstützung durch das Programm NSERC CREATE DREAMS der Dalhousie University. Die Verfasser danken Dr. Ling Li von BASF für die Bereitstellung der Elektrolytlösemittel und -salze. Dank geht auch an Dr. Larry Krause von 3M für die hilfreichen Gespräche.
The authors acknowledge the support of this work under the auspices of the NSERC/3M Canada Industrial Research Chair in Materials for Advanced Batteries. LED and KJN acknowledge financial support from the NSERC CREATE DREAMS program at Dalhousie University. The authors thank Dr. Jing Li of BASF for providing the electrolyte solvents and salts. Useful discussions with Dr. Larry Krause at 3M are acknowledged.
Hier klicken, um eine Druckversion dieses Anwendungsartikels herunterzuladen.

