Productos | Microcalorímetros | RS-DSC de TA Instruments
RS-DSC de TA Instruments
La última generación de pruebas de estabilidad térmica para fármacos biológicos
El RS-DSC (calorímetro diferencial de Barrido, de Escaneo Rápido, Rapid Screening-Differential Scanning Calorimeter) de TA Instruments es un instrumento potente y versátil que revoluciona las pruebas de estabilidad térmica de fármacos biológicos. Con su alta eficiencia y análisis optimizado, el RS-DSC de TA Instruments ayuda al personal de los laboratorios biofarmacéuticos a tomar decisiones más informadas y al mismo tiempo acelerar el tiempo de comercialización.

El RS-DSC de TA Instruments puede ayudar a
- Acelerar las pruebas de estabilidad térmica: El RS-DSC de TA Instruments proporciona información detallada sobre la estabilidad térmica de los productos farmacéuticos significativamente más rápido al analizar hasta 24 muestras de manera simultánea. La tecnología del RS-DSC de TA Instruments también simplifica la caracterización de productos farmacéuticos altamente concentrados.
- Mejorar la eficiencia: El RS-DSC de TA Instruments asegura que los materiales se usen con eficiencia al utilizar MFC (chips microfluídicos, Micro Fluidic Chips) desechables para contener la muestra. Los MFC requieren un volumen de muestra de <15 µl, y el diseño facilita la operación más limpia y optimizada al reducir la necesidad de dilución tediosa de muestras y de limpieza repetitiva de instrumentos, así como los riesgos de contaminación.
- Tomar decisiones más informadas: El software NanoAnalyze™ maneja sin esfuerzo el volumen de datos aumentado producido por el RS-DSC de TA Instruments, y proporciona información detallada y precisa acerca de la estabilidad térmica y las propiedades termodinámicas de una molécula.

Propuestas de valor
- Rendimiento mejorado: el RS-DSC de TA Instruments permite el análisis de 24 muestras a la vez, lo que acelera significativamente la investigación, así como la entrada al mercado de fármacos biológicos.
- Eficiencia de recursos: los requisitos mínimos de volumen de muestra del RS-DSC de TA Instruments ayudan a asegurar el uso máximo de material y a minimizar los costos.
- Competencia en alta concentración: el RS-DSC de TA Instruments tiene un desempeño sobresaliente al probar un extenso rango de concentraciones de muestras, y una capacidad singular para analizar de manera eficiente y efectiva productos farmacológicos de muy alta concentración.
- Flujo de trabajo simplificado: El RS-DSC de TA Instruments optimiza las operaciones al eliminar la necesidad de diluir la muestra cuando se trabaja con muestras de alta concentración, y los chips microfluídicos desechables reducen o eliminan la necesidad de limpieza y disminuyen el riesgo de contaminación.
- Análisis integral de datos: el software NanoAnalyze maneja datos y proporciona información detallada para optimizar el desarrollo.
Características y beneficios
- Análisis paralelo: el análisis exclusivo de alto rendimiento permite hasta 24 mediciones simultáneas para acelerar la investigación.
- Tecnología microfluídica de un solo uso: los MFC optimizan la operación al simplificar la caracterización de productos farmacológicos de alta concentración; asimismo, reducen el tiempo de limpieza y los riesgos de contaminación.
- Software de análisis de datos de última generación: el software NanoAnalyze, robusto y fácil de usar, analiza los datos de manera automática y consistente para la evaluación a profundidad y rápida.
| RS-DSC | |
| Geometría de celda | Microfluídica desechable |
| Material de la celda | Vidrio |
| Formato de la muestra | MFC (chips microfluídicos, Micro Fluidic Chips) |
| Volumen de trabajo de la celda | 11 µl |
| Capacidad de muestra | 24 MFC |
| Concentración típica de la muestra | 20 mg/ml a más de 330 mg/ml de IgG (dependiente de proteína)1 |
| Rendimiento de muestras | > 96 muestras/día |
| Rango de temperatura | 20 a 100 °C |
| Velocidad de escaneo de temperatura | 1 o 2 °C/min |
| Precisión de temperatura | ± 0.2 °C (en todos los calorímetros); reproducibilidad ± 0.1 °C2 |
2 Al usar DPPC en agua a pH de 7 a 1 °C/min Acelere la investigación, mejore la eficiencia y tome decisiones más informadas con el RS-DSC de TA Instruments, un nuevo y revolucionario instrumento de prueba de estabilidad térmica, de alto rendimiento, diseñado específicamente para el desarrollo de fármacos biológicos.
Tecnología
Capacidades innovadoras
Tecnología microfluídica: el futuro de la precisión y la comodidad
Equipado con MFC (chips microfluídicos, Micro Fluidic Chips), de última generación, el RS-DSC de TA Instruments está diseñado para contener la muestra sin esfuerzo. Esta integración tecnológica elimina la necesidad de limpieza repetitiva de la celda de medición del instrumento entre ejecuciones, lo que ahorra tiempo, disminuye el riesgo de contaminación y permite lecturas más precisas y confiables.
Los MFC son desechables y mejoran la facilidad operativa; permiten transiciones rápidas, y protegen el instrumento de sustancias peligrosas. El novedoso diseño de MFC ejemplifica tecnología de vanguardia, de bajo volumen y de un solo uso, que facilita la carga y preparación de muestras con equipo de laboratorio estándar. Una muestra se puede preparar, sellar y dejar lista para el análisis en menos de un minuto, y solo se requieren volúmenes mínimos para la evaluación precisa.
Ver demostración del producto
Aplicaciones
El RS-DSC de TA Instruments es ideal para una amplia gama de aplicaciones en el desarrollo de fármacos biológicos, incluso:
La estabilidad térmica es un indicador principal del éxito clínico general de un producto farmacológico biológico, y la DSC (calorimetría diferencial de barrido, Differential Scanning Calorimetry) es una herramienta primaria que se utiliza para caracterizar el efecto del entorno de la solución sobre la estabilidad de las proteínas. Los efectos sobre la estabilidad de las proteínas pueden reflejarse en cambios pequeños de Tmáx o en cambios de hasta decenas de grados resultantes de la alteración de variables como el pH, el amortiguador, la fuerza iónica, los excipientes y los detergentes sobre la estabilidad de la proteína.
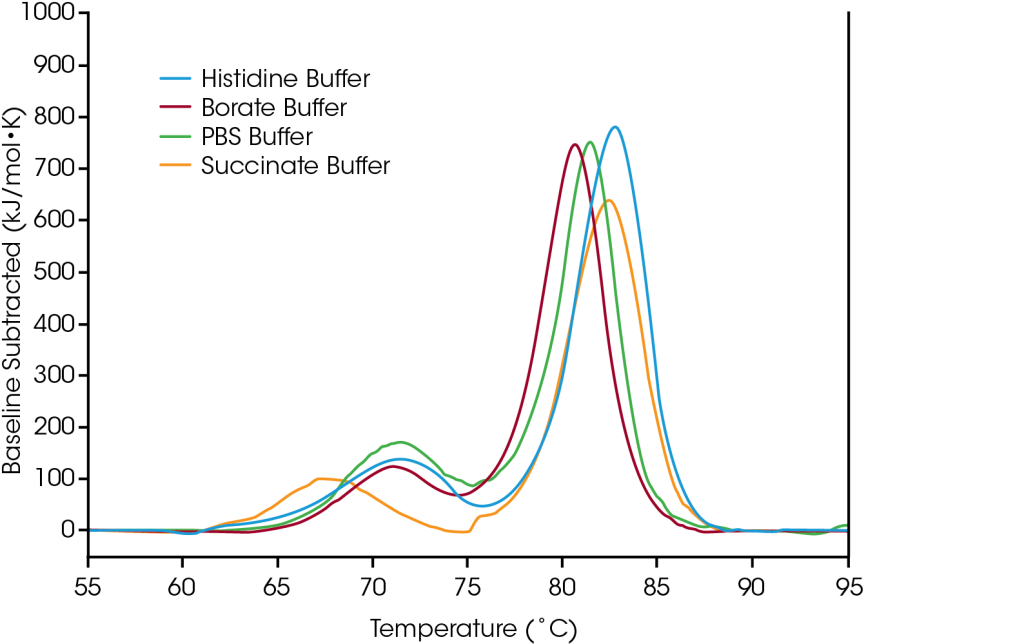
Para demostrar cómo los datos provenientes del estudio de la formulación pueden ayudar en la selección de los componentes del amortiguador, el anticuerpo trastuzumab se probó en cuatro condiciones de amortiguador comunes: 1) un amortiguador de trabajo común (PBS), 2) un amortiguador que permite la conjugación con lisina para la síntesis de anticuerpos marcados para estudios de tráfico celular o conjugación de fármacos (borato), 3) un conjugado de fármaco-anticuerpo basado en trastuzumab (succinato) y 4) el amortiguador de formulación natural para trastuzumab (histidina).Los amortiguadores de histidina, borato o PBS no afectan significativamente
el primer evento de despliegue, correspondiente al despliegue del dominio CH2. Sin embargo, el amortiguador succinato desestabiliza el dominio CH2, lo que da por resultado disminución del inicio del despliegue y Tmáx,1 aproximadamente 3 °C. Con respecto a la transición principal que refleja los eventos de despliegue de Fab y CH3, los amortiguadores histidina y succinato son los más estabilizadores, con una Tmáx,2 de 82.66 °C. La transición principal es menos estable en el amortiguador de borato con una Tmáx,2 de 80.69 °C. Como es de esperar, la formulación de amortiguador más estabilizadora para trastuzumab en este conjunto de muestras es el amortiguador de histidina utilizado para la formulación final del producto farmacológico aprobado.
Las mutaciones de proteína son una estrategia común para optimizar su estructura y función, e incluso las modificaciones de un solo aminoácido pueden tener un efecto mensurable en la estabilidad general de la proteína. El uso de DSC (calorimetría diferencial de barrido, Differential Scanning Calorimetry) para ayudar en la caracterización de modificaciones de proteínas diseñadas es esencial para comprender las repercusiones estructurales de la mutación sobre la proteína en su conjunto, y puede ayudar a guiar la toma de decisiones en el proceso de desarrollo de fármacos biológicos. Para demostrar los tipos de efectos que la modificación de la secuencia pueden tener sobre la estabilidad, se analizó un pequeño panel de proteínas diseñadas para detectar cambios de la estabilidad térmica originados por mutaciones de un solo aminoácido en la secuencia de la proteína.
En la proteína parental, el despliegue se produce dentro de una transición térmica principal a una Tmáx de 75.92 °C. Se hizo una mutación de un solo aminoácido que no tiene un efecto importante sobre la estabilidad térmica a corto plazo (mutación 1); sin embargo, se ha demostrado que mutaciones de un solo aminoácido alternativas tienen repercusiones significativas sobre la estabilidad de la proteína (mutación 2 y mutación 3). Como se ilustra en la desestabilización importante en la mutación 3, la modificación no siempre tiene el mismo efecto, sino que más bien depende tanto del lugar donde se encuentra como de las propiedades fisicoquímicas del nuevo aminoácido. Optimizar los beneficios funcionales deseados de la modificación de secuencia con la estabilidad estructural de la proteína en su conjunto ayuda a comprender la relación estructura-función, y puede facilitar el desarrollo de terapéuticas avanzadas.
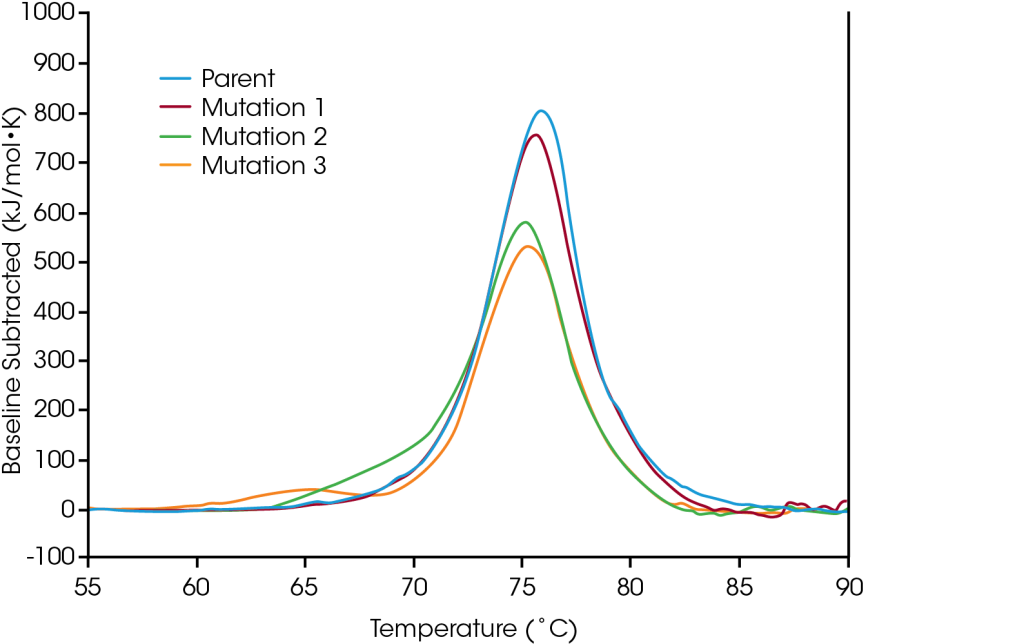
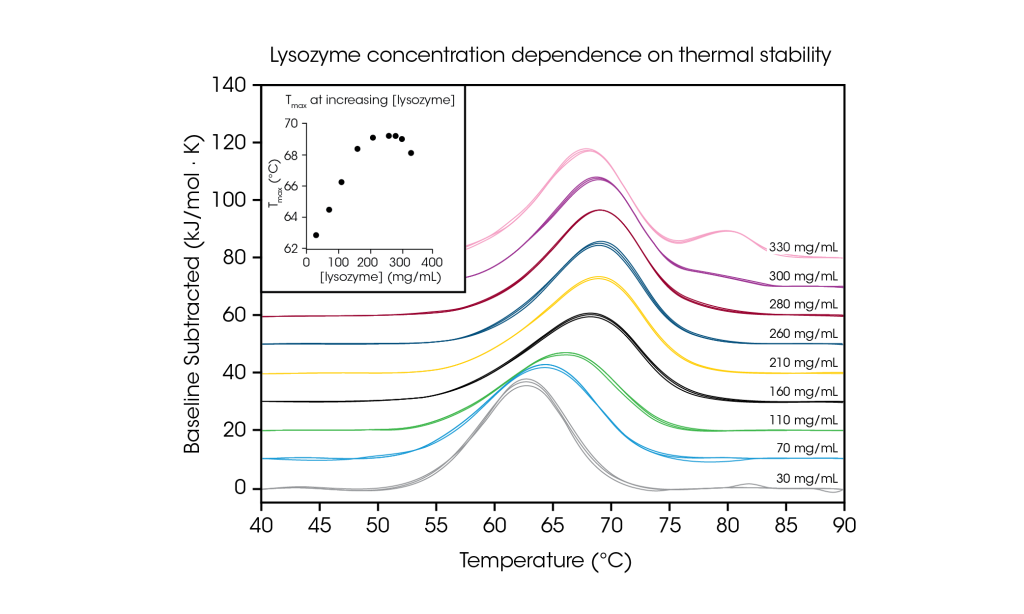
El RS-DSC de TA Instruments está especialmente diseñado para manejar muestras de fármacos biológicos de alta concentración, con un enfoque especializado en fármacos anticuerpos, y conjugados de fármacos con anticuerpos. Con el éxito creciente de la terapéutica con anticuerpos, en la industria farmacéutica hay interés aumentado en formas de dosificación de alta concentración que permitan la administración de fármacos por vía subcutánea y ocular. Por consiguiente, las formulaciones con concentraciones de 50 a 150 mg/ml de anticuerpos son comunes y pueden llegar hasta más de 200 mg/ml. La formulación de proteínas a concentraciones altas puede aumentar la susceptibilidad a la inestabilidad física. Por el contrario, en algunos estudios de casos se ha demostrado una mejora de la estabilidad térmica a concentraciones aumentadas. De este modo, la comprensión del despliegue térmico y la respuesta al entorno de la solución a la concentración de formulación de interés es un parámetro esencial para aminorar la responsabilidad por el producto farmacológico.
Para demostrar la capacidad de analizar muestras de proteínas de alta concentración e ilustrar la importancia de realizar pruebas en la concentración de formulación deseada, evaluamos la lisozima de clara de huevo de gallina de 30 a 330 mg/ml en amortiguador de glicina. Con un termograma de transición única simple a concentraciones bajas (~1 mg/ml), la lisozima se usa comúnmente como una muestra de prueba de referencia para DSC. Mediante la evaluación de concentraciones de proteína hasta 100 veces más altas, observamos que la estabilidad de la lisozima tuvo dependencia de la concentración.
Recursos
- Nota de aplicación: Rapid Thermal Stability Screening of High Concentration Biologic Drugs
- Nota de aplicación: Rapid Thermal Stability Screening and Selection of Monoclonal Antibody Drug Products
- Demostración de Producto: Introducing the RS-DSC: A Dilution-Free Method for Screening Thermal Stability of High Concentration Biotherapeutics








