Produits | Microcalorimétrie | RS-DSC de TA Instruments
RS-DSC de TA Instruments
La nouvelle génération de tests de stabilité thermique pour les médicaments biologiques
Le RS-DSC (Calorimètre à balayage différentiel pour le dépistage rapide) de TA Instruments est un instrument puissant et polyvalent qui révolutionne les tests de stabilité thermique des médicaments biologiques. Grâce à sa grande efficacité et à son analyse rationalisée, le RS-DSC de TA Instruments aide les laboratoires biopharmaceutiques à prendre des décisions plus éclairées tout en accélérant la mise sur le marché.

Le RS-DSC de TA Instruments peut aider à
- Accélérer les tests de stabilité thermique: Le RS-DSC de TA Instruments fournit des informations détaillées sur la stabilité thermique des produits pharmaceutiques beaucoup plus rapidement en analysant jusqu’à 24 échantillons simultanément. La technologie du RS-DSC de TA Instruments simplifie également la caractérisation des produits pharmaceutiques hautement concentrés.
- Améliorer l’efficacité: Le RS-DSC de TA Instruments garantit une utilisation efficace des matériaux en utilisant des MFC (Micro Fluidic Chips) jetables pour contenir l’échantillon. Les MFC nécessitent un volume d’échantillon 15ul, et leur conception facilite une opération plus propre et plus rationnelle en réduisant la nécessité d’une dilution fastidieuse de l’échantillon, le nettoyage répétitif des instruments et les risques de contamination.
- Prendre des décisions plus éclairées: Le logiciel NanoAnalyze™ traite sans effort le volume de données accru produit par le RS-DSC de TA Instruments, ce qui permet d’obtenir des informations approfondies et précises sur la stabilité thermique et les propriétés thermodynamiques d’une molécule.

Des capacités révolutionnaires
- Débit amélioré: Le RS-DSC de TA Instruments permet d’analyser 24 échantillons simultanément, ce qui accélère considérablement la recherche et la mise sur le marché des médicaments biologiques.
- Efficacité des ressources: Les exigences minimales du RS-DSC de TA Instruments en matière de volume d’échantillon permettent de maximiser l’utilisation des matériaux et de minimiser les coûts.
- Efficacité à haute concentration: Le RS-DSC de TA Instruments excelle dans le test d’une gamme étendue de concentrations d’échantillons et possède une capacité unique d’analyse efficace des produits pharmaceutiques à très haute concentration.
- Flux de travail simplifié: Le RS-DSC de TA Instruments rationalise les opérations en supprimant la nécessité de diluer les échantillons quand ces derniers sont à forte concentration, et les puces microfluidiques jetables réduisent, voire éliminent la nécessité d’un nettoyage et réduisent le risque de contamination.
- Analyse complète des données: Le logiciel NanoAnalyze gère les données et fournit des informations détaillées pour optimiser le développement.
Caractéristiques et avantages
- Analyse parallèle: L’analyse unique à haut débit permet d’effectuer jusqu’à 24mesures simultanées afin d’accélérer la recherche.
- Technologie microfluidique à usage unique: Les MFC rationalisent les opérations en simplifiant la caractérisation des produits pharmaceutiques à haute concentration et en réduisant le temps de nettoyage et les risques de contamination.
- Logiciel d’analyse de données de pointe: Le logiciel NanoAnalyze, robuste et convivial, analyse automatiquement et régulièrement les données pour une évaluation approfondie et rapide.
| RS-DSC | |
| Géométrie des cellules | Microfluidique à usage unique |
| Matériau de la cellule | Verre |
| Modèle de format | MFC (puces microfluidiques) |
| Volume de la cellule de travail | 11 µL |
| Capacité de l’échantillon | 24 MFC |
| Concentration typique de l’échantillon | 20 mg/mL – 330+ mg/mL IgG (dépendant de la protéine)1 |
| Débit d’échantillons | > 96 échantillons/jour |
| Intervalle de températures | 20-100 °C |
| Taux de balayage de la température | 1 ou 2 °C/min |
| Précision de la température | ± 0,2 °C (pour tous les calorimètres) ; reproductibilité ± 0,1 °C2 |
2 Utilisation de DPPC dans l’eau à pH 7 à 1 °C/min Accélérez la recherche, améliorez l’efficacité et prenez des décisions plus éclairées avec le RS-DSC de TA Instruments, un nouvel instrument révolutionnaire de test de stabilité thermique à haut débit spécialement conçu pour le développement de médicaments biologiques.
Technologie
Des capacités révolutionnaires
Technologie microfluidique: l’avenir de la précision et de la commodité
Équipé de MFC (puces microfluidiques) de pointe, le RS-DSC de TA Instruments est conçu pour contenir l’échantillon sans effort. Cette intégration technologique élimine le besoin de nettoyage répétitif de la cellule de mesure de l’instrument entre les tests, ce qui permet de gagner du temps, de réduire le risque de contamination et d’obtenir des lectures plus précises et plus fiables.
Les MFC sont jetables et facilitent les opérations en permettant des transitions rapides et en protégeant l’instrument des substances dangereuses. La nouvelle conception de la MFC est un exemple de technologie de pointe, à faible volume et à usage unique, qui facilite le chargement et la préparation des échantillons avec un équipement de laboratoire standard. Un échantillon peut être préparé, scellé et prêt pour l’analyse en moins d’une minute, et ne nécessite que des volumes minimes pour une évaluation précise.
Regardez la démonstration du produit
Applications
Le RS-DSC de TA Instruments est idéal pour une large gamme d’applications dans le domaine du développement de médicaments biologiques, notamment :
La stabilité thermique est un indicateur majeur du succès clinique global d’un médicament biologique, et la DSC (calorimétrie différentielle à balayage) est l’un des principaux outils utilisés pour caractériser l’effet de l’environnement de la solution sur la stabilité des protéines. Les effets sur la stabilité des protéines peuvent se traduire par de petits déplacements du Tmax ou par des changements allant jusqu’à des dizaines de degrés résultant de la modification de variables telles que le pH, le tampon, la force ionique, les excipients et les détergents sur la stabilité des protéines.
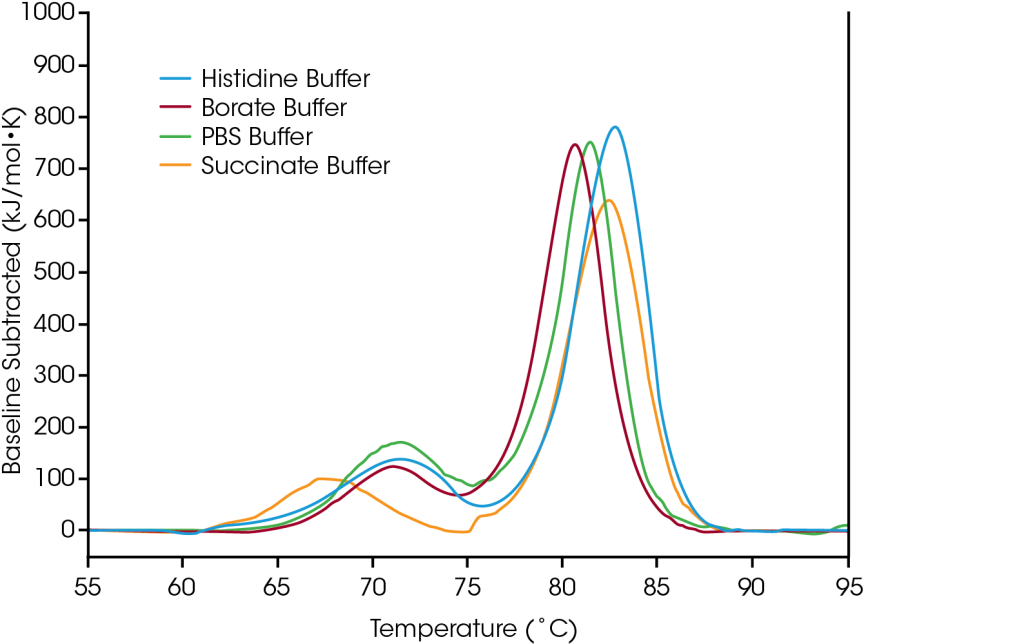
Pour démontrer comment les données issues du criblage de la formulation peuvent aider à la sélection des composants du tampon, l’anticorps trastuzumab a été testé dans quatre conditions de tampon courantes: 1) un tampon de travail commun (PBS), 2) un tampon qui permet la conjugaison avec la lysine pour la synthèse d’anticorps marqués en vue d’études sur le trafic cellulaire ou la conjugaison avec des médicaments (borate), 3) un anticorps conjugué avec des médicaments à base de trastuzumab (succinate), et 4) le tampon de formulation natif pour le trastuzumab (histidine).
Le premier événement de dépliage, correspondant au dépliage du domaineCH2, n’est pas significativement affecté par les tampons histidine, borate ou PBS. Cependant, le tampon succinate déstabilise le domaine CH2, ce qui entraîne une diminution du début du dépliage et de Tmax,1 d’environ 3°C. En ce qui concerne la transition principale reflétant les événements de dépliage Fab et CH3, les tampons histidine et succinate sont les plus stabilisants, avec une Tmax,2 de 82,66°C. La transition principale est la moins stable dans le tampon borate avec une Tmax,2 de 80,69°C. Sans surprise, la formulation tampon la plus stabilisante pour le trastuzumab dans cet ensemble d’échantillons est le tampon d’histidine utilisé pour la formulation finale du produit pharmaceutique approuvé.
Les mutations protéiques sont une stratégie courante pour optimiser la structure et la fonction des protéines, et même les modifications d’un seul acide aminé peuvent avoir un effet mesurable sur la stabilité globale de la protéine. L’utilisation de la DSC (calorimétrie différentielle à balayage) pour aider à la caractérisation des modifications des protéines est essentielle pour comprendre l’impact structurel de la mutation sur la protéine dans son ensemble et peut aider à guider la prise de décision dans le pipeline de développement des médicaments biologiques. Pour démontrer les types d’effets que la modification de la séquence peut avoir sur la stabilité, un petit panel de protéines modifiées a été examiné pour déterminer les changements de stabilité thermique qui résultent de mutations d’un seul acide aminé dans la séquence de la protéine.
Dans la protéine mère, le dépliage se produit au cours d’une transition thermique majeure à une Tmax de 75,92°C. La mutation d’un seul acide aminé n’a pas d’effet majeur sur la stabilité thermique à court terme (Mutation 1); cependant, d’autres mutations d’un seul acide aminé ont un impact significatif sur la stabilité de la protéine (Mutation2 et Mutation3). Comme l’illustre la déstabilisation significative de la Mutation3, la modification n’a pas toujours le même effet, car ce dernier dépend à la fois du site de la modification et des propriétés physicochimiques du nouvel acide aminé. L’optimisation des avantages fonctionnels souhaités de la modification de la séquence avec la stabilité structurelle de la protéine dans son ensemble aide à comprendre la relation structure-fonction et peut faciliter le développement de thérapies avancées.
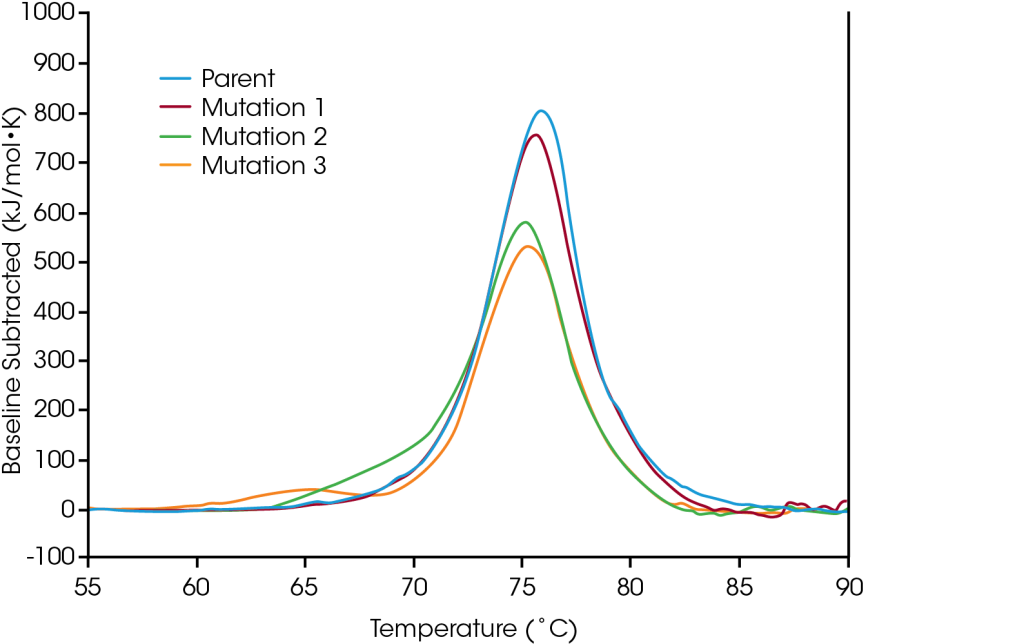
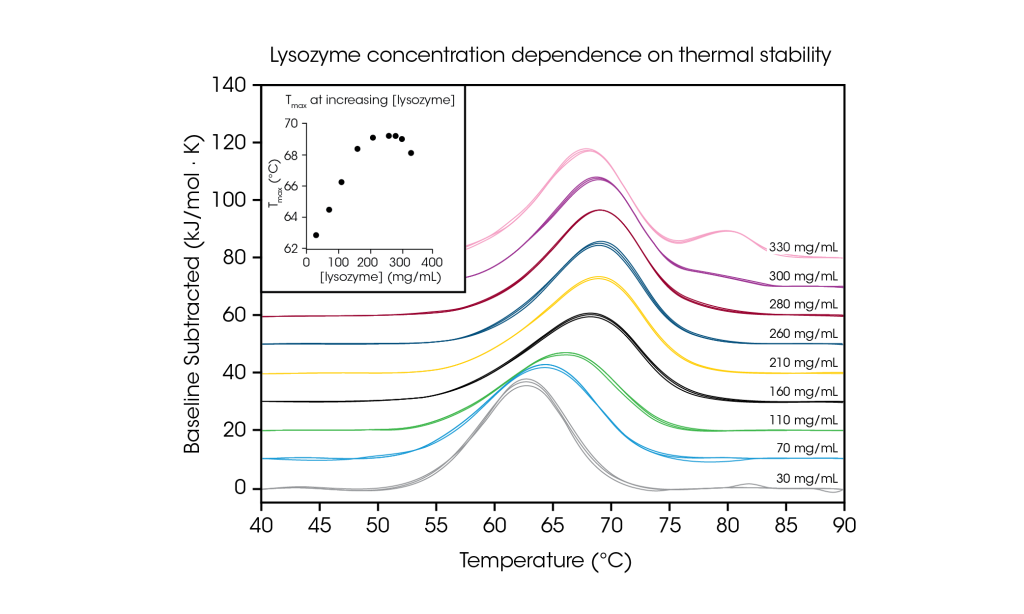
Le RS-DSC de TA Instruments est spécialement conçu pour traiter des échantillons de médicaments biologiques à haute concentration, avec une attention particulière pour les anticorps et les conjugués anticorps-médicaments. Avec le succès croissant des thérapies à base d’anticorps, l’industrie pharmaceutique s’intéresse de plus en plus aux formes de dosage à haute concentration qui permettent l’administration de médicaments par voie sous-cutanée et oculaire. Ainsi, les formulations avec des concentrations de 50 à 150mg/mL d’anticorps sont courantes et peuvent aller jusqu’à plus de 200mg/mL. La formulation de protéines à des concentrations élevées peut accroître la susceptibilité à l’instabilité physique. Inversement, certaines études de cas ont montré une amélioration de la stabilité thermique à des concentrations plus élevées. Ainsi, la compréhension du dépliement thermique et de la réponse à l’environnement de la solution à la concentration de formulation d’intérêt est une mesure critique pour atténuer le risque des produits pharmaceutiques.
Pour démontrer la capacité à tester des échantillons de protéines à haute concentration et illustrer l’importance de tester la concentration de formulation souhaitée, nous avons évalué le lysozyme de blanc d’œuf de poulet de 30 à 330mg/mL dans un tampon de glycine. Avec un thermogramme de transition simple à de faibles concentrations (~1mg/mL), le lysozyme est couramment utilisé comme échantillon de référence pour la DSC. En évaluant des concentrations de protéines jusqu’à 100fois plus élevées, nous avons observé une dépendance de la concentration sur la stabilité du lysozyme.
Ressources
- Note d’application: Rapid Thermal Stability Screening of High Concentration Biologic Drugs
- Note d’application: Rapid Thermal Stability Screening and Selection of Monoclonal Antibody Drug Products
- Démonstration du produit: Présentation de la RS-DSC : une méthode sans dilution pour tester la stabilité thermique des produits biothérapeutiques à haute concentration








